
카테고리: 원하는 부분만 골라! 골라!
순서: 남들이 많이 봤던 내용들만 먼저! 먼저!
키워드 검색: 원하는 내용만 뽑아! 뽑아!
카르노사이클 열효율, 단열관계식 적용 (Molar heat capacity)
Ch. 4 Energy Analysis of Closed Systems
작성자
kwonjunpyo
작성일
2020-06-17 04:29
조회
1849

Cp - Cv = nR 의 관계식이 성립하고,
감마 = Cp/Cv라 했을때, 저 사진 속 문제의 감마는
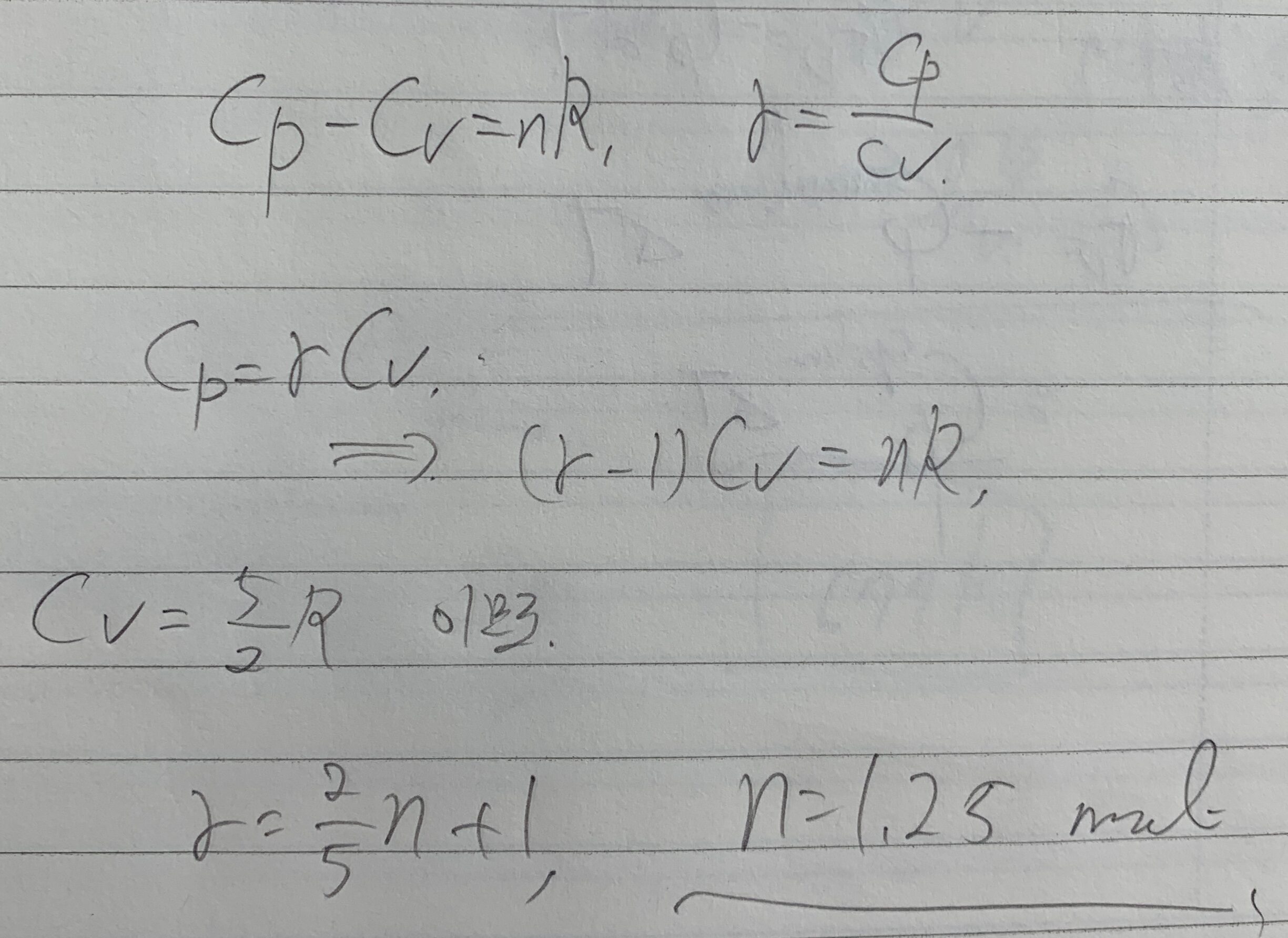
요런 과정으로 나올수가 있는데 문제에서 주어진 n 값을 넣으면 감마가 1.5, n을 무시하면 위 답지처럼 1.4가 나옵니다. 근데 식에 명백히 나온 n을 무시할 수가 있나요..?
Thermodynamics – An Engineering Approach, Cengel & Boles, McGrawHill
Ch. 1 Introduction and Basic Concepts
Ch. 2 Energy, Energy Transfer, and General Energy Analsysis
Ch. 3 Properties of Pure Substances
Ch. 4 Energy Analysis of Closed Systems
Ch. 5 Mass and Energy Analysis of Control Volumes
Ch. 6 The Second Law of Thermodynamics
Ch. 7 Entropy
Ch. 8 Exergy
Ch. 9 Gas Power Cycles
Ch. 10 Vapor and Combined Power Cycles
Ch. 11 Refrigeration Cycles
Ch. 12 Thermodynamic Property Relations
Ch. 13 Gas Mixtures
Ch. 14 Gas-Vapor Mixtures and Air-Conditioning
Ch. 15 Chemical Reactions
Ch. 16 Chemical and Phase Equilibrium
Ch. 17 Compressible Flow
- “열역학 한방에 끝내기” 는 초등학생도 이해할 수 있게끔 쉽고 재미있게 열역학을 설명하고 있습니다.
- 공식만 외워서 문제를 푸는 방식은 올바른 역학 공부법이 아니고, 조금만 응용된 문제가 나오면 접근하기가 매우 어려워져 좋은 시험 점수(좋은 학점)을 받기가 매우 어려워집니다.
- 원리와 원칙에 충실하여 어떤 문제가 나와도 개념에 충실해서 풀 수 있어야 학업성취도, 취업 면접, 대학원 시험 등에서 좋은 결과를 기대할 수 있습니다.
단열 과정임을 이용해서 부피를 계산하는 것은 아시는 것 같은데
단열비에 대해서 질문을 주신 것 같습니다.
보통 Cv 또는 Cp 라고 하면
기본적으로 생각할 때 the molar heat capacity 라고 생각하는 것이 맞습니다.
때문에 Cp-Cv=nR이라는 식에서 n이 있으면 안되겠습니다.
그렇다면 왜 n이 문제에 있는지가 의문인데,
혹시 뒤에 다른 문제들이 더 있는지 모르겠습니다.
질문내용이 불완전하여 답변드리기 어려운 부분이 있습니다.
아울러 그림이 없어서 일단 문제를 읽고 아래와 같이 풀이했으니
한 번 살펴보시길 바랍니다.
혹시라도 제가 문제를 잘못 이해했다면 알려주시길 바랍니다.
감사합니다.
Thanks!!!
위에 풀이에서
d->a: adiabatic expansion 이 아니라 adiabatic compression 입니다.
오타가 있어 아래와 같이 수정합니다.