
카테고리: 원하는 부분만 골라! 골라!
순서: 남들이 많이 봤던 내용들만 먼저! 먼저!
키워드 검색: 원하는 내용만 뽑아! 뽑아!
상태량 구하기
Ch. 4 Energy Analysis of Closed Systems
작성자
hjung0215
작성일
2020-10-21 16:09
조회
3161
복학하기 전에 가지고 제가 전공 서적과 교수님 강의로 역학 복습 중입니다.
과제로 오해받을 까봐 ... 혹시 몰라서 적어 놓았습니다.
질문 1>

문제를보고 Q_in이 내부 압력이 증가 하겠구나! 라고 가정을하고 문제를 접근했다가
풀수있는 방법이 없어서 가정 자체가 잘못 됬나하고 솔루션을 보니
P_2 = P_1 = P_atm + P_piston 이라고하고 문제를 접근 하더군요 ... (등압 과정)
보통 열이 증가하면 압력이 증가해야하는 하는걸로 알고 있는데..
이문제에서는 그것이 자유로이 움직일 수있어서 압력의 평형을 이루어서 그런가 라는 생각도 해보았습니다.
어떤 원리로 P_2 = P_1 = P_atm + P_piston 이런 접근이 나온 건가요 ??
등압으로 풀어야하는 어떤 조건이 따로 있는건가요?
질문2>

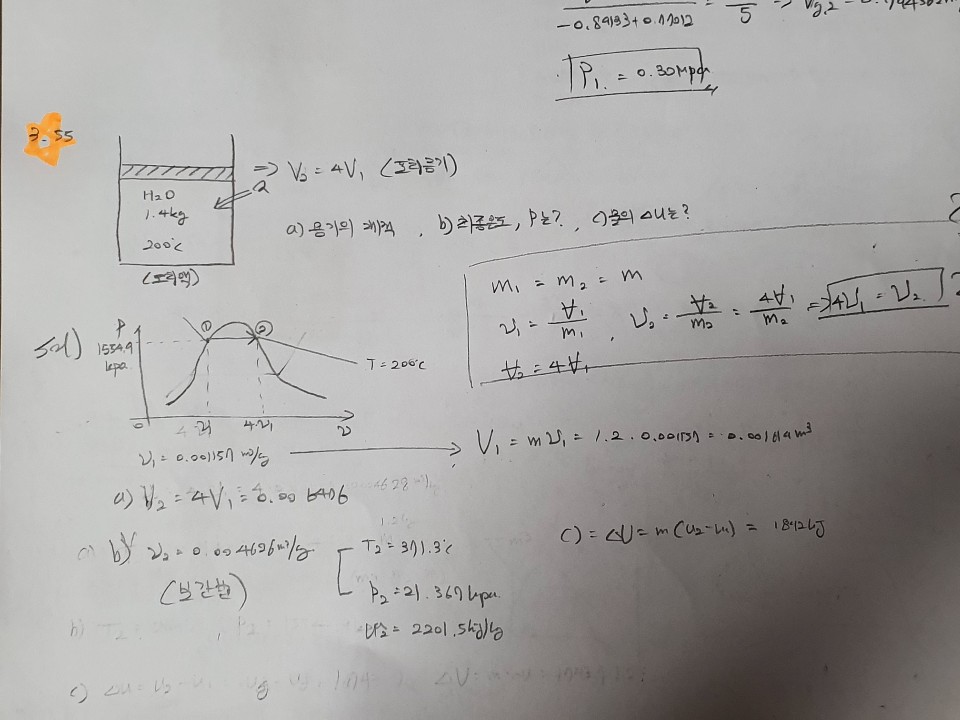
위 문제는 포화액이 전부 포화증기가 될때 포화액상태의 체적의 4배가 된다고 합니다.
그래서 포화액 질량과 포화증기 질량이 같다라고 놓고 포화액 상태의 비체적 (v_f)* 4를 하고 난뒤에
질량을 곱해주어서 포화증기일때의 체적을 구했습니다.
(포화증기 상태의 비체적 * 4 *m )
그리고 나서 포화액 상태에서 포화증기로 완전히 변했을때의 온도,압력을 구하라고 했으니
당연히 등온 등압과정으로 상변화 할테니
T_1.satliquid = T_2.satgas, P_1.satliquid = P_2.satgas
라고 접근하여 풀었습니다. 근데 역시나 틀렸습니다.
어떤한 포화액이 포화증기로 변환될때에 위 풀이에 그려진 과정같이 수행되어야 하는거 아닌가요??
그리고 위 질문1번 문제와 비슷한 감이 있는데 왜 1번문제는 등압이고 2번문제는 등압이 아닌가요?
질문 2>
 총 용기에서 초기 상태가 T = 200, m = 1.4kg 인 포화 액이 포화 증기로 바있다 때의 상태량들을 구하는 문제입니다.
총 용기에서 초기 상태가 T = 200, m = 1.4kg 인 포화 액이 포화 증기로 바있다 때의 상태량들을 구하는 문제입니다.
처음 접근을 용기의 25 %의 포화 액이 전부 포화 증기로 변환될때 온도와 압력을 구하는 것이니 T_1.satliquid = T_2.satgas, P_1.satliquid = P_2.satgas 라고 생각을하고 접근을 했습니다.
근데 솔루션을 확인해 보니 잘못된 접근이었습니다 ..
pv, tv 선도에서 포화 액에서 포화로 상 변화시에는 온도, 압력이 일정하게 유지 되는 되야하는 거라고?
왜 압력과 온도가 포화증기일때 증가한건가요?
질문에 두서가 없어서 죄송합니다 ..
과제로 오해받을 까봐 ... 혹시 몰라서 적어 놓았습니다.
질문 1>

문제를보고 Q_in이 내부 압력이 증가 하겠구나! 라고 가정을하고 문제를 접근했다가
풀수있는 방법이 없어서 가정 자체가 잘못 됬나하고 솔루션을 보니
P_2 = P_1 = P_atm + P_piston 이라고하고 문제를 접근 하더군요 ... (등압 과정)
보통 열이 증가하면 압력이 증가해야하는 하는걸로 알고 있는데..
이문제에서는 그것이 자유로이 움직일 수있어서 압력의 평형을 이루어서 그런가 라는 생각도 해보았습니다.
어떤 원리로 P_2 = P_1 = P_atm + P_piston 이런 접근이 나온 건가요 ??
등압으로 풀어야하는 어떤 조건이 따로 있는건가요?
질문2>


위 문제는 포화액이 전부 포화증기가 될때 포화액상태의 체적의 4배가 된다고 합니다.
그래서 포화액 질량과 포화증기 질량이 같다라고 놓고 포화액 상태의 비체적 (v_f)* 4를 하고 난뒤에
질량을 곱해주어서 포화증기일때의 체적을 구했습니다.
(포화증기 상태의 비체적 * 4 *m )
그리고 나서 포화액 상태에서 포화증기로 완전히 변했을때의 온도,압력을 구하라고 했으니
당연히 등온 등압과정으로 상변화 할테니
T_1.satliquid = T_2.satgas, P_1.satliquid = P_2.satgas
라고 접근하여 풀었습니다. 근데 역시나 틀렸습니다.
어떤한 포화액이 포화증기로 변환될때에 위 풀이에 그려진 과정같이 수행되어야 하는거 아닌가요??
그리고 위 질문1번 문제와 비슷한 감이 있는데 왜 1번문제는 등압이고 2번문제는 등압이 아닌가요?
질문 2>

 총 용기에서 초기 상태가 T = 200, m = 1.4kg 인 포화 액이 포화 증기로 바있다 때의 상태량들을 구하는 문제입니다.
총 용기에서 초기 상태가 T = 200, m = 1.4kg 인 포화 액이 포화 증기로 바있다 때의 상태량들을 구하는 문제입니다.처음 접근을 용기의 25 %의 포화 액이 전부 포화 증기로 변환될때 온도와 압력을 구하는 것이니 T_1.satliquid = T_2.satgas, P_1.satliquid = P_2.satgas 라고 생각을하고 접근을 했습니다.
근데 솔루션을 확인해 보니 잘못된 접근이었습니다 ..
pv, tv 선도에서 포화 액에서 포화로 상 변화시에는 온도, 압력이 일정하게 유지 되는 되야하는 거라고?
왜 압력과 온도가 포화증기일때 증가한건가요?
질문에 두서가 없어서 죄송합니다 ..
Thermodynamics – An Engineering Approach, Cengel & Boles, McGrawHill
Ch. 1 Introduction and Basic Concepts
Ch. 2 Energy, Energy Transfer, and General Energy Analsysis
Ch. 3 Properties of Pure Substances
Ch. 4 Energy Analysis of Closed Systems
Ch. 5 Mass and Energy Analysis of Control Volumes
Ch. 6 The Second Law of Thermodynamics
Ch. 7 Entropy
Ch. 8 Exergy
Ch. 9 Gas Power Cycles
Ch. 10 Vapor and Combined Power Cycles
Ch. 11 Refrigeration Cycles
Ch. 12 Thermodynamic Property Relations
Ch. 13 Gas Mixtures
Ch. 14 Gas-Vapor Mixtures and Air-Conditioning
Ch. 15 Chemical Reactions
Ch. 16 Chemical and Phase Equilibrium
Ch. 17 Compressible Flow
- “열역학 한방에 끝내기” 는 초등학생도 이해할 수 있게끔 쉽고 재미있게 열역학을 설명하고 있습니다.
- 공식만 외워서 문제를 푸는 방식은 올바른 역학 공부법이 아니고, 조금만 응용된 문제가 나오면 접근하기가 매우 어려워져 좋은 시험 점수(좋은 학점)을 받기가 매우 어려워집니다.
- 원리와 원칙에 충실하여 어떤 문제가 나와도 개념에 충실해서 풀 수 있어야 학업성취도, 취업 면접, 대학원 시험 등에서 좋은 결과를 기대할 수 있습니다.
안녕하세요.
질문도 깔끔하게 잘 올려주시고,
무엇보다
비슷한 예제를 바탕으로
다양하게 이해해보려는 모습이
너무 바람직하고 보기 좋습니다.
이런 식으로 공부하시면
매우 좋은 학습이 될 겁니다.
다양하게 생각해보시고 고민해보세요.
저는 위의 세 문제를 보면서 아래와 같이 정리했습니다.
- 첫 번째 문제: Superheated, No phase change (열역학 1법칙의 기본)
- 두 번째 문제: Isobaric but phase change (피스톤이기 때문에 등압과정인 것은 동일)
- 세 번째 문제: Isochoric but phase change (sat.상태라는 전제 때문에 두 번째 문제와 동일)
아래의 사진과 같이
첫 번째 문제풀이를 먼저 보시면 좋겠습니다.
위의 풀이에서
등압과정인 것이 이해가 안 된다면,
갓준표 사이트에 있는
피스톤 문제를 모두 풀어보시길 바랍니다.
상태량표는 아래와 같이 참조했습니다.
두 번째 문제의 경우,
상태량이 변화하기 때문에
superheated 가 아닌
saturated 테이블을 보는 것이 핵심입니다.
사실, 처음과 나중(1번과 2번)의 부피 변화 정보를 통해
v2만 계산할 수 있다면,
sat. vapor라는 가정을 이용해
상태량표를 바탕으로
쉽게 나머지 값들을 구할 수 있으십니다.
두 번째 문제에서 참조한 상태량표 1
두 번째 문제에서 참조한 상태량표 2
세 번째 문제는
우연인지 모르겠지만
두 번째 문제와 완전히 동일합니다.
더욱이 sat. 상태라는 가정도 있어서
사실 isochoric이 갖고 있는 문제의 특성을
잘 살리지 못한
쉬운 문제로 보여집니다.
원래 rigid box로 문제가 나오면
가장 먼저 의심해봐야 할 내용이 건도인데,
여기서는 건도를 고려할 필요가 없어서
사실 두 번째 문제와
다를 것이 없어 보입니다.
(갓준표 사이트에 rigid box 문제가 많으니 꼭 풀어보세요!)
솔루션이 있다면 더욱 제가 확실하게 풀 수 있을텐데
맞는지는 정확하게 모르겠습니다.
하지만,
일단 saturated이라는 가정을 통해
두 번째 문제와 다를 것이 없다고 생각합니다.
아래의 풀이를 살펴보세요.
혹시 솔루션이 있다면
아래에 첨부해주실 수 있나요?
그리고 이 문제에 대해서는
역학 콘서트에서 한번 다루면 좋을 것 같습니다.
솔루션이 확보되어서
답이 정확하게 맞는지 확인한 후
역학 콘서트에서 추가 강의로 설명드릴 수 있도록 하겠습니다.
좋은 질문해주셔서 감사합니다.
열심히 공부하세요.
그리고 학생분의 질문 중에
sat. value를 이용해서 많이 푸시는 것을 발견했는데,
상태량표에서 sat. value는 보통
문제의 조건 상에서의 물질의 상태가
- saturated인지
- superheated인지를
판별할 때 주로 쓰입니다.
상태량표에서 결과값을 계산할 때에는
실제 문제에서 제공되는 정보를 이용해서
보간법으로 풀어낸다는 점을
기억하시면 좋겠습니다.
솔루션 아래에 첨부했습니다!
제가 교수님께서 주신 답을 보고 다시 한번 풀어보았는데요.
아직까지 궁금증이 풀리지 않아 몇가지 질문드릴려고 합니다!
3*-27번 문제
피스톤-실린더가 등압과정이다라고 가정하고 해석을 하는 이유를 제가 나름 이해만큼 적어보자면
열량의 유입으로 온도가 증가하면서 P_in이 P_atm+P_P_piston보다 커지게되고 실린더 체적이 증가하게 되는데
이때 P_in의 값이 P_atm+P_P_piston와 같아질때까지 실린더 체적이 증가함 따라서 최종단계에서는 실린더의 내부 압력과 외부대기압 + 무게의 압력과 동일시 되기 때문에 등압과정이라고 봐도 무방하다.
다만 ligid box의 경우 체적이 일정한 상태에서 열량이 들어가게되면 내부에너지 즉 분자의 활성도가 증가하기 때문에
온도가 증가하고 압력이 증가하게된다. 이때 피스톤과 달리 압력을 평형 상태로 조절할수 없기때문에 열량 유입이 중단될때까지 온도와 압력이 증가한다.
여기까지가 제가 내린 결론입니다.
근데 제가 좀 햇갈리는게 P_in이 증가를 하게되면 체적과 압력은 반비례이기 때문에 팽창이 아니라 압축이 되어야하는게
아닌가 싶기도하고.. P_in자체가 실린더를 밀어내는 방향으로 작용하기 때문에 팽차을 하는건지 햇갈립니다..
제가 몬가 쉬운 개념을 놓치고있는 기분이 드는데... 이게 몰까요..
그리고 문제3-55도 피스톤 실린더 기구이면은 등압과정(P_i = P_f)으로 문제를 접근해야 하는데 그렇다는 거는 P-v선도를 그려봤을때 아래처럼 과정이 진행이 되어야 하는데 아닌가요? 그니깐
문제에서 구한 포화증기의 비체적에 해당하는 P가 왜 초기상태의 P와 다른 이유가 알고 싶습니다.
문제 5-27과 다른점이 과열증기, 포화액 -> 포화증기에서의 상변화만 다른점이라고 보이는데 이두 과정에서 어떤 차이있어서 그러는건지.. 아니면 여기서도 몬가 잘못 이해하고 있는건지, 쉬운개념이 어디서 빠진건지 잘모르겠습니다....
지금까지 생각한 바로는 등압이니깐 온도가 T_2까지 상승했으니
T_1일떄의 그래프가 T_2일때의 그래프까지 올렸을때 구한 포화증기의 비체적과 겹치는 곳이 P_2이다
라고 생각을 해봤는데 아닌것 같고..
온도와 체적은 증가하지만 압력은 일정하다 가 등압과정아닌가요?
이 등압과정이라는게 초기에서 최종상태까지 압력이 일정해야하는게 아닌가 라는 생각도 해봤는데 그렇다고 하기에는 3-27번 문제가 걸리고..
지금 어디서 막혔는지 감이 잡히질 않습니다.. 이럴경우에는 어떻게 해야하나요??
요 한 2틀정도 계속 고민해도 점점 미궁으로 빠지는 느낌이 들고있습니다.
생각이 자꾸 꼬여서 질문에 두서가 없는것같아 죄송합니다.
답변주시면 정말로 감사하겠습니다!
그래프
3-27
첨부파일 : 3-27.PNG
3-55
첨부파일 : 3-55.PNG
3-57
첨부파일 : 3-57.PNG